How Mitochondria Produce Energy
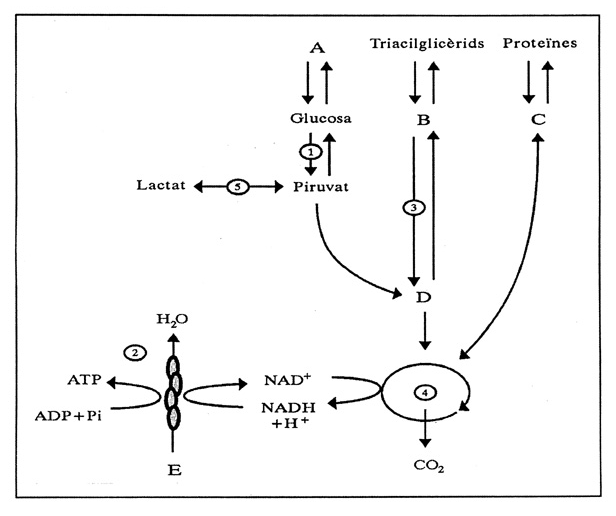
Esquema general del metabolisme cel·lular
Amb aquest esquema es pot repassar d’una manera global les vies catabòliques i anabòliques. Un bon punt d’inici per repassar els detalls importants de cadascuna d’elles.
Fosforilació oxidativa en la cadena respiratòria
Aquí està la presentació que es va passar a classe i que donava suport a l’explicació de la fosforilació oxidativa. He redissenyat la presentació en format vídeo.
Cicle dels àcids tricarboxílics (CAT)
Aquí està la presentació que es va passar a classe i que donava suport a l’explicació del cicle de Krebs. He redissenyat la presentació en format vídeo. Els números corresponen a les reaccions indicades en el llibre de text.
Pas previ al CAT: transformació del piruvat en acetilCoA
Aquí està la presentació que es va passar a classe i que donava suport a l’explicació de la transformació del piruvat a acetil CoA, pas previ al cicle de Krebs. He redissenyat la presentació en format vídeo. Els números corresponen a les reaccions indicades en el llibre de text.
La glicòlisi
Aquí està la presentació que es va passar a classe i que donava suport a l’explicació de la via catabòlica de la glicòlisi. He redissenyat la presentació en format vídeo. Els números corresponen a les reaccions indicades en el llibre de text.
I en el següent vídeo podeu veure en més detalls les diferents fases:
Activitat enzimàtica
Els enzims són biocatalitzadors, i per tant acceleren les reaccions bioquímiques que tenen lloc en les diferents rutes metabòliques que es duen a terme en les cèl·lules. De fet, els enzims redueixen l’energia d’activació que és necessària subministrar als substrats perquè la reacció es doni en el sentit de la formació dels productes.
La cinètica de l’activitat enzimàtica està ben definida per l’equació de Michaelis-Menten:
V=Vmax · [S] / km + [S]
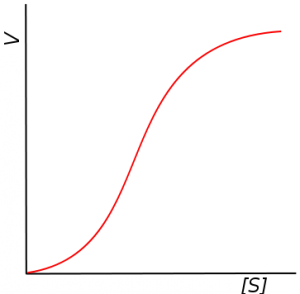
i la expressió gràfica és la següent:
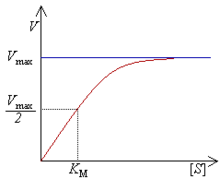
Creat: Uploaded by Magnus Manske on en.wikipedia 14:27, August 27, 2002
A concentracions baixes de substrat (i amb una concentració constant d’enzim), aquest li es fàcil trobar el lloc actiu de l’enzim i per tant la reacció és molt ràpida. Per a aquests valors de substrat la velocitat de reacció és proporcional i es manifesta amb una recta. Seria una situació en que [E]>[ES]: tot el substrat està “col·locat” en el centre actiu de l’enzim formant el complex ES.
A mesura que augmenta la concentració de substrat, aquest es pot trobar de forma majoritària formant els complexos ES, però també algunes molècules de substrats lliures i algunes molècules d’enzims amb el centre actiu lliure. Per això en la gràfica, l’augment de la velocitat ja no és tant fort, segueix una línia corba creixent. Seria la situació en què [ES]>[E]
Finalment, a concentracions molt elevades de substrat la velocitat de reacció s’aproxima a un valor màxim i s’estabilitza (no augmenta). En aquest cas tots els enzims tenen el centre actiu ocupat pels substrats i ara és necessari que hagin d’esperar “torn” per ocupar el centre actiu de l’enzim, perquè ja està ocupat i ha de finalitzar la reacció catalítica. Seria la situació en què [S]>[ES]>[E].
Interpreteu gràfiques (i esquemes) de la cinètica de l’activitat enzimàtica
Gràfica 1:
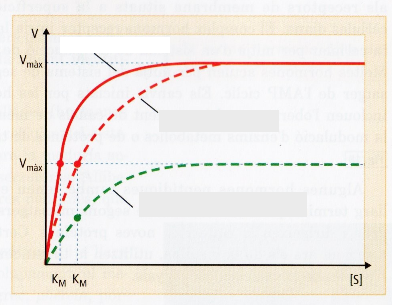
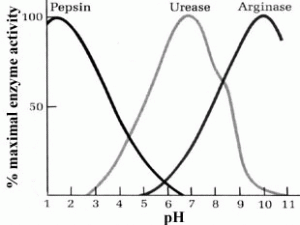
Gràfica 2:
Gràfica 3:
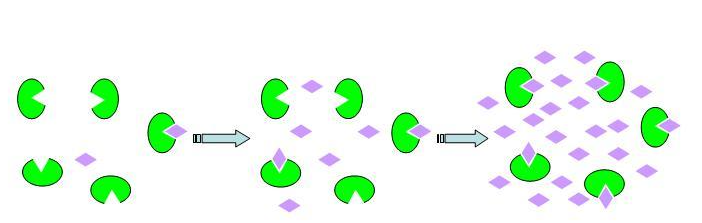
Esquema 4: