Unitat didàcta: El llenguatge de la química
1-Objectius
- Saber formular i interpretar les fórmules químiques.
- Saber formular en diferents nomenclatures (Stock, clàssica i sistemàtica)
- Saber diferenciar entre òxids, hidrurs, àcids, bases, àcids i sals.
2-La representació de la materia
Els elements s’agrupen formant compostos i per representar-los es necessari utilitzar fórmules químiques.Per formular seguirem la normativa de l’ IUPAC (Unión Internacional de Química Pura y Aplicada) que es va formar el 1919 per homogeneïtzar la formulació química.
3-Nombre d’oxidació
El nombre d’oxidació d’un element en un compost és un nombre enter, amb signe positiu o negatiu, que depen del nombre d’electrons que participi en l’enllaç. Un mateix element pot presentar diferents nombres d’oxidació segons el compost del qual formi part.
En aquesta taula pots veure diferents nombres d’oxidació dels elements de la taula periòdica.
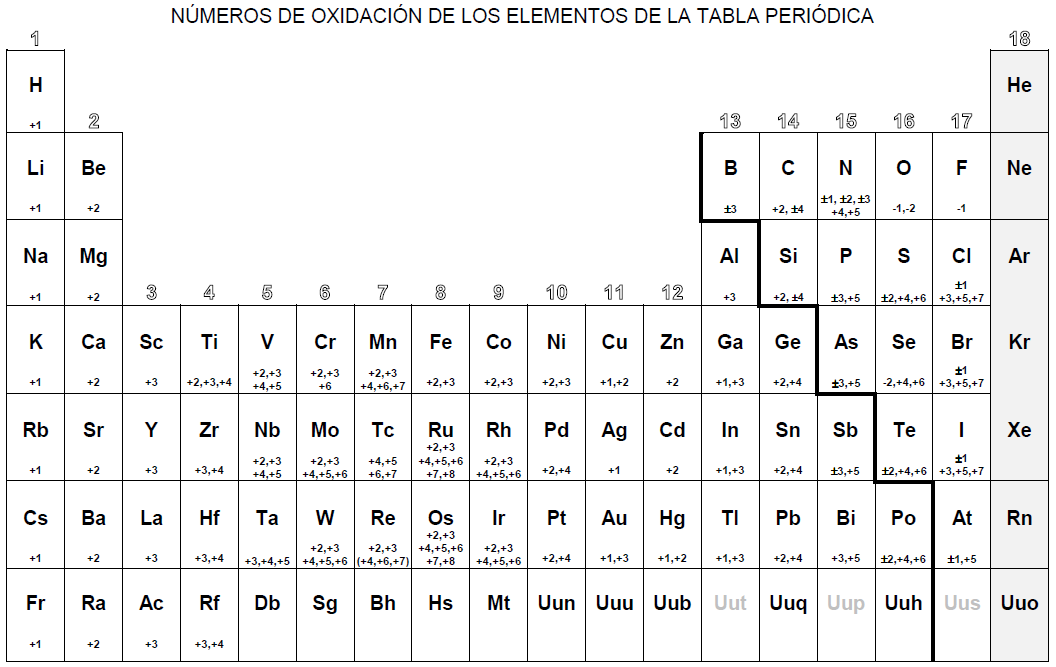
- El nombre d’oxidació es positiu si l’element perd electrons ( metalls per exemple)
- El nombre d’oxidació serà negatiu si guanya electrons, en general els no metalls.
- Si el nombre d’oxidació no li posem signe i el representem per nombres romans (I,II,III,..) s’anomena valència.
Per exemple 
El nombre d’oxidació del alumini és +3 i la valència III, el nombre d’oxidació de l’oxígen -2 i la seva valència II.
- Un mateix element pot tenir més d’un nombre d’oxidació, i de signes diferents.
- Per exemple:
En l’aigua oxigenada el nombre d’oxidació de l’oxígen és -1 i en l’aigua -2.
- Pot tenir varis nombres d’oxidació amb el mateix signe

El ferro actúa amb valències III i II, els nombres d’oxidació seran +3 i +2.
Mira aquest vídeo per tenir les idees més clares(1)
[youtube]http://youtu.be/BA2zUg1MsHM[/youtube]
4-Formulació i nomenclatura dels compostos inorgànics
- Per formular adequadament cal conèixer els nombres d’oxidació.Els més habituals són:
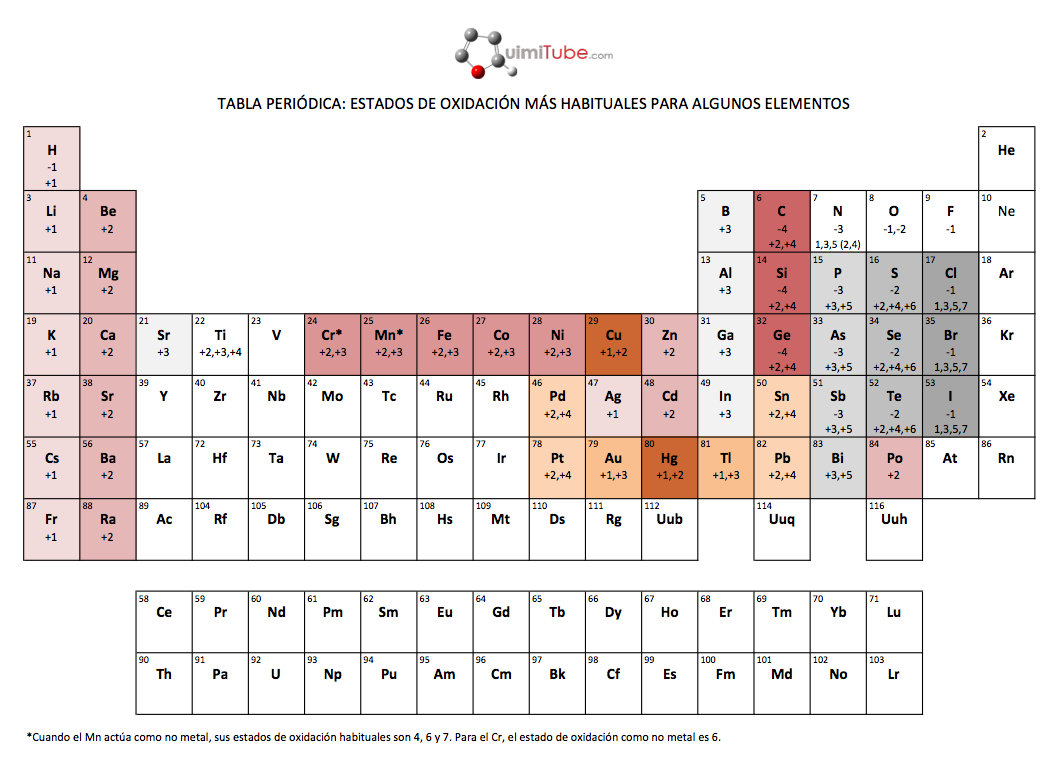
- La suma dels nombres d’oxidació de tots els àtoms dels elements que intervenen en un compost ha de ser zero.
4.1.Regles per trobar el nombre d’oxidació:
- Un element lliure és zero: Metalls: Cu, Fe, etc gasos diatòmics (O2, H2,…)
- En general el nombre d’oxidació de l’oxigen és -2, excepte aigua oxigenada (i peròxids), quan es combina amb el fluor que serà +2.
- El nombre d’oxidació de l‘hidrogen serà +1, excepte amb els hidrurs metàlics que serà -1 (HLi).
- Els alcalins el nombre d’oxidació serà +1 (Li, Na, K…)
- Els alcalins-terris el nombre d’oxidació serà +2 (Be, Ca,…)
- El grup dels halogens si formen hidràcids el nombre d’oxidació serà -1, i el grup del del sofre si formen hidràcids -2.
- La suma de tots els nombres d’oxidació es zero.Si es vol trobar quin és la valència del sofre en aquest compost:
 Hem de partir que el sodi és sempre +1, l’oxígen és -2,per que la suma de 2.(+1)+4.(-2) doni zero implica que el sofre té valència +6.els nombre que apareixen davant del nombre d’oxidació són el nombre d’àtoms de sodi i d’oxigen que hi ha.
Hem de partir que el sodi és sempre +1, l’oxígen és -2,per que la suma de 2.(+1)+4.(-2) doni zero implica que el sofre té valència +6.els nombre que apareixen davant del nombre d’oxidació són el nombre d’àtoms de sodi i d’oxigen que hi ha.
5-Compostos binaris
S’anomenen compostos binaris al formats per dos elements:
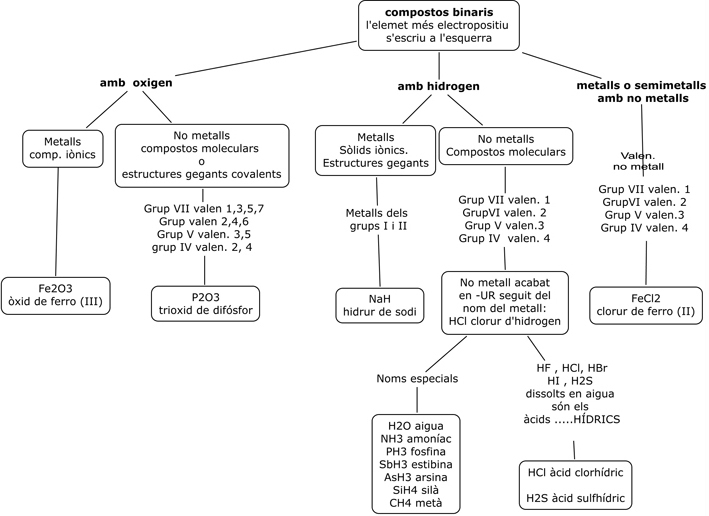
Compostos formats per dos elements(binaris)
5.1-Òxids
Són els compostos que es combinen amb l’oxigen, aquest té de nombre d’oxidació -2.
Hi ha tres tipus de formulació:
5.1.1.Nomenclatura Stock
S’anomena òxid de….i el nom de l’element i entre parèntesis la valència.Si té una sola valència no cal posar-la.Per exemple NaO= òxid de sodi, Fe2O3=òxid de ferro (III).
5.1.2.Nomenclatura antiga o clàssica
a)Si el element que es combina amb l’oxigen te una valència : és posa el sufix -ic
NaO=òxid sòdic
b)Si el element que es combina amb l’oxigen te dos valències
- -ós per a la valència més petita
- -ic per a la valència més gran
FeO=òxid ferrós
Fe”O3=ôxid fèrric
c)Si el element que es combina amb l’oxigen te tres valències
- Hipo-… -Ós per a la valència més petita
- -Ós per a la valència petita
- -Ic per a la valència gran
SO=òxid hiposulfurós
SO2=òxid sulfurós
SO3=òxid sulfúric
d)Si el element que es combina amb l’oxigen te quatre valències
- Hipo-… -Ós per a la valència més petita
- -Ós per a la valència petita
- -Ic per a la valència gran
- Per-… -Ic per a la valència més gran
ClO=òxid hipoclorós
Cl2O3=òxid clorós
Cl2O5=òxid clòric
Cl2O7=òxid perclòric
5.1.3.Nomenclatura Sistemàtica
Es forma fent servir un prefix numeral seguit de l’arrel -òxid de, un segon prefix numeral i el nom de l’element.
Fe2O3=triòxid de diferro
5.1.4.Exemples per practicar
a)Mira aquest quadre on trobares exemples.
| ormulació | Nomenclatura de Stock | Nomenclatura sistemàtica | Nomenclatura antiga |
|---|---|---|---|
| FeO | òxid de ferro (II) | monòxid de ferro | òxid ferrós |
| Fe2O3 | òxid de ferro (III) | triòxid de dihierro (sesquiòxid de ferro) | òxid fèrric |
| Cl2O | òxid de clor (I) | monòxid de diclor | anhídrid hipoclorós |
| Cl2O3 | òxid de clor (III) | triòxid de diclor | anhídrid clorós |
| Cl2O5 | òxid de clor (V) | pentòxid de diclor | anhídrid clòric |
| Cl2O7 | òxid de clor (VII) | heptaòxid de diclor | anhídrid perclòric |
b)Pots practicar en webs
http://www.edu365.cat/eso/muds/ciencies/formulacio/fitxers/oxidsmarcs.htm
En castellà pots practicar en les webs següents
http://www.latizavirtual.org/quimica/quim_ino.html
c)Pots jugar:
http://www.juanjoeldefisica.com/FYQ/tic_tac_toe/tic_tac_toe_binarios.htm
http://www.juanjoeldefisica.com/FYQ/snakes_and_ladders/snakes_and_ladders.htm
5.2.Hidrurs
Es coneixen amb aquest nom els composts resultants de la combinació de l’hidrogen amb un altre element qualsevol. Per facilitar la seva nomenclatura, els podem dividir en:
5.2.1-Hidrurs metàlics
Combinació d’hidrògen més metall.L’hidrogen es posarà a la dreta- S’anomenen com:
a) Di, tri, tetra….. hidrur de……. nom del metall.
b) Hidrur de …..nom del metall (valència)
hidrur de sodi NaH trihidrur de ferro o hidrur de ferro(III) FeH3 tetrahidrur d’estany o hidrur d’estany(IV) SnH4 5.2.2.Hidrurs no metàlics
Es la combinació de l’hidrogen i un no metall. L’hidrogen es posarà a la esquerra si es tracta del grup VII i VI, si es tracta del III IV i V es posarà a la dreta.
5.2.2.1-Grup VII i VI, s’anomenen …….-ur d’hidrogen si es tracta d’un gas i àcid ……clorhídric si està en dissolució.L’hidrogen a la esquerra.Actuen amb el nombre d’oxidació més petit.
fluorur d’hidrogen àcid fluorhídric HF sulfur de dihidrogen o sulfur d’hidrogen àcid sulfhídric H2S clorur d’hidrogen àcid clorhídric HCl 5.2.2.2-Grup V , IV i III,S’anomenen com tri, tetra,… hidrur de (element).o bé amb el seu nom propi.L’hidrogen es posa a la dreta.
| trihidrur de bor o hidrur de bor o borà | BH3 |
| tetrahidrur de carboni o metà | CH4 |
| tetrahidrur de silici o silà | SiH4 |
| trihidrur de nitrogen o amoníac |
NH3 |
| trihidrur de fòsfor o hidrur de fòsfor(III) o fosfà | PH3 |
| trihidrur d’arsènic o arsà | AsH3 |
| trihidrur d’antimoni o estibà | SbH3 |
Exercicis per practicar:
http://www.xtec.cat/~rblanco1/exerauto/Index_Formulacio.htm
Exemples
http://www.acienciasgalilei.com/qui/formulacion/hidruros%20metalicos.htm
Us d’alguns hidrurs:
5.3-Compostos metall+ no metall
El metall actua amb nombre d’oxidació positiu i el no metall negatiu.
S’anomenen fent acabar l’arrel del no metall en ur i a continuació el nom del metall, especificant el nombre d’oxidació, prefixos multiplicadors o el nombre de càrrega.
A l’hora de formular-los, el metall s’escriu a l’esquerra.
| Fe3N2 | Dinitrur de triferro/Nitrur de ferro(II) |
| PbI4 | Tetraiodur de plom/Iodur de plom (IV) |
| KBr | Bromur de potassi/Bromur de potassi |
5.4-Compostos no metall+ no metall
El no metall més electronegatiu (d’acord amb la llista de sota) actua amb nombre d’oxidació negatiu i l’altre amb nombre d’oxidació positiu.
B, Si, C, Sb, As, P, N, H, Te, Se, S, At, I, BR, Cl, O, F
S’anomenen fent acabar en ur l’arrel del no metall més electronegatiu i a continuació el nom de l’altre element especificant el seu nombre d’oxidació si cal.
| carbur de silici | SiC |
| triclorur de fòsfor o clorur de fòsfor(III) | PCl3 |
| disulfur de carboni o sulfur de carboni(IV) | CS2 |
| pentasulfur de diarsènic | As2S5 |
6-Hidròxids
Estan formats per la unió d’un metall amb l’ió hidròxid= OH– (actua amb nombre d’oxidació .S’anomenen hidròxid de….. i el nom del metall especificant el nombre d’oxidació.
| hidròxid de calci o dihidròxidde calci | Ca(OH)2 | ||
| hidroxid d’amoni | NH4OH | ||
| hidròxid de sodi | NaOH | ||
| trihidròxid de ferro | hidròxid de ferro(III) | Fe(OH)3 | |
| dihidròxid de níquel | hidròxid de níquel(II) | Ni(OH)2 |
7-Àcids
Dins aquest apartat es tenen que considerar els hidràcids (hidrurs no metàl·lics en dissolució) estudiats abans i els àcids formats a partir d’un òxid més aigua, que ‘anomena oxiàcids.Són compostos de fórmula general HxMyOz, on M és un element no metàl·lic o bé un metall de transició amb estat d’oxidació elevat (per exemple, Cr o Mn).
7.1-Oxiàcids
Es té que tenir en compte per la nomenclatura clàssica els nombre d’oxidació
| Nombres d’oxidació | ||||
| hipo…ós | ós | -ic | per…………ic | |
| Halògens (Cl, Br, I) | +1 | +3 | +5 | +7 |
| Amfígens (S, Se, Te) | +2 | +4 | +6 | |
| Nitrogenoides (N, P, As, Sb) | +3 | +5 | ||
| Carbonoides (C, Si) | +4 | |||
| Bor | +3 | |||
| Crom | +6 | |||
| Manganès | +6 | +7 | ||
Per obtenir les fórmules posarem l’òxid simplificat més aigua.
- L’hidrogen té estat d’oxidació +1 i l’oxigen -2.
- L’element M té l’estat d’oxidació positiu.
- Grup VII: Valències I,III,V i VII
(I) Cl2O + H2O -> HClO àcid hipoclorós
(III) Cl2O3 + H2O -> HClO2 ácid clorós
(V) Cl2O5 + H2O -> HClO3 ácid clóric
(VII) Cl2O7 + H2O -> HClO4 ácid perclóric
- Grup VI:Valències:II,IV i VI
(II) SO + H2O -> H2SO2 àcid hiposulfuros
(IV) SO2 + H2O -> H2SO3 àcid sulfuros
(VI) SO3 + H2O -> H2SO4 àcid sulfúric
- Grup V: III i V
El nitrogen forma dos àcids:
Pensa quin sera el nom d’aquests àcids en català.
El fosfor i l’arsènic donen àcids especials.
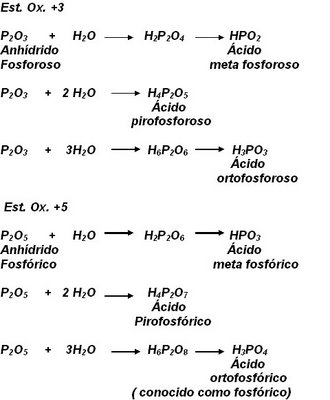
Com pots observar si afegim un aigua l’àcid s’anomena meta…, dos aigues piro…, i tres aigues orto…
- Grup IV:IV
(IV) CO2 + H2O -> H2CO3 àcid carbónic
(IV) SiO2 + H2O -> H2SiO3 àcid silícic
- Grup III
- El bor es pot polihidratar i agafar una, dos o tres aigues.
- B2O3 +H2O—— H2B2O4 = HBO2 ÀCID METABORÓSB2O3 +2H2O—— H4B2O5 ÀCID PIROBORÓSB2O3 +3H2O—— H6B2O6 = H3BO3 ÀCID ORTOBORÓS
No només es formulen els àcids de aquesta forma cLàssica sino com els òxids, de forma sistemàtica i Stock , observa aquest quadre D’AQUESTA PÀGINA WEB
http://www.bioygeo.info/pdf/Oxoacidos.pdf
En Internet hi ha molt vídeos que os poden ajudar aquí teu un:
[youtube]http://youtu.be/od0uC_KPOGo[/youtube]
- Hi ha dos metalls que són el crom i el manganès que poden donar àcid i aquest són:
CrO3 + H2O = H2CrO4 àcid cròmic (valència VI)
Cr2O6 +H2O = H2Cr2O7 acid decròmic (valència VI)
MnO3 + H2O = H2MnO4 àcid mangànic (valència VI)
Mn2O7 + H2O = H2Mn2O8 =HMnO4 àcid permangànic (valència VII)
7.2-Exercicis per treballar
http://www.latizavirtual.org/quimica/quim_ino.html
Test: http://www.eis.uva.es/~qgintro/genera.php?tema=1&ejer=6
http://www.xtec.cat/~rblanco1/exerauto/Index_Formulacio.htm
7.3-Ús dels àcid
Els àcids inorgànics s’utilitzen com a substàncies químiques intermèdies i catalitzadors en reaccions químiques. Es troben en diferents indústries, com metalistería, fusta, tèxtils, colorants, petroli i fotografia. En el treball dels metalls s’utilitzen sovint com a agents netejadors abans de soldar o pintar.
L’àcid nítric s’utilitza en la fabricació de nitrat amònic per a fertilitzants i explosius.
[youtube]http://youtu.be/S-bihg-IOYU[/youtube]
Àcid sulfúric, H2SO4 és l’àcid que s’empra en major quantitat, s’empra en la indústria química per a la preparació d’altres àcids, de sulfats i de carbonats. En la producció de pintures, sulfonació de greixos, en la indústria tèxtil, en la refineria del petroli, en la producció de ferro i acer.
[youtube]http://youtu.be/32meed7kD7c[/youtube]
Àcid clorhídric,HCl.Es fa servir com decapat de l’acer, l’acidificació de pous de petroli, la fabricació d’aliments, la producció de clorur de calci i el tractament de minerals.
L’àcid clorhídric és important en el cos humà, degrada els aliments perque pugui ser absorbit.El seu pH és de 1 a 2, aquest àcidesa desfa els metalls, pero l’estomac està protegit per una mucosa que evita l’atac de l’àcid.