HIPÒTESIS D’AVOGADRO
Hipòtesi segons la qual, en condicions idèntiques de pressió i temperatura, volums iguals de gasos diferents contenen el mateix nombre de molècules.
UN MOL
MASSA MOLAR
DISSOLICIONS
En una dissolució s’anomena dissolvent el compost que es troba en més proporció i al de menys s’anomena solut.
Una propietat de la dissolució es la concentració, que es la quantitat de solut que hi ha en una dissolució.
- Diluidas. Cuando la cantidad de soluto respecto al solvente es muy pequeña. Por ejemplo: 1 gramo de azúcar en 100 gramos de agua.
- Concentradas. Cuando la cantidad de soluto respecto al solvente es grande. Por ejemplo: 25 gramos de azúcar en 100 gramos de agua.
- Saturadas. Cuando el solvente no acepta ya más soluto a una determinada temperatura. Por ejemplo: 36 gramos de azúcar en 100 gramos de agua a 20 °C.
- Sobresaturadas. Como la saturación tiene que ver con la temperatura, si incrementamos la temperatura, se puede forzar al solvente a tomar más soluto del que ordinariamente puede, obteniendo una solución sobresaturada (saturada en exceso, digamos). Así, sometida a un calentamiento, la solución tomará mucho más soluto del que ordinariamente podría.
– Fuente: https://concepto.de/solucion-quimica/
FORMES DE CALCULAR LA CONCENTRACIÓ
La concentració és una magnitud que descriu la relació que hi ha entre el solut i el dissolvent.
Es pot epressar;
- %Peso/peso. Se expresa en gramos de soluto sobre gramos de solución.
- %Volumen/volumen. Se expresa en centímetros cúbicos (cc) de soluto sobre cc de solución.
- %Peso/volumen. Combina las dos anteriores: gramos de soluto sobre cc de solución.
Unidades químicas. Aquellas que se expresan en sistemas de unidades químicas. Por ejemplo:
- Molaridad (M). Se expresa en número de moles de soluto sobre un litro de solución o un kilogramo de solución. Se calcula de la siguiente manera:
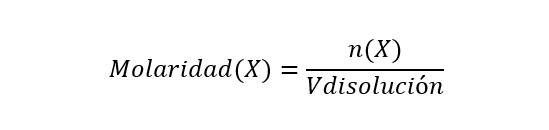
Donde n(X) es la cantidad de moles del componente X y Vdisolución es el volumen de la disolución. La molaridad se expresa en moles/Ldisolución.
- Fracción molar (Xi). Se expresa en términos de moles de un componente (solvente o soluto) en relación con los moles totales de la solución, de la siguiente manera:
Xsolución = moles de soluto / (moles de soluto + moles solvente)
Xsolvente = moles de solvente / (moles de soluto + moles solvente)
Siempre contemplando que:
Xsolvente + Xsolución = 1
La fracción molar es adimensional, es decir, no se expresa en unidades de medición.
- Molalidad (m). Es la proporción entre el número de moles de cualquier soluto disuelto por kilogramos de disolvente. Se calcula de la siguiente manera:
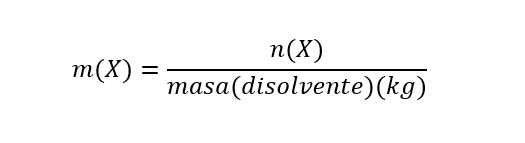
Donde m(X) es la molalidad de X, n(X) es el número de moles de X y masa(disolvente) es la masa de disolvente expresada en kg. Es importante aclarar que la molaridad se expresa por kg (1000g) de disolvente. Se expresa en unidades de mol/kg.
– Fuente: https://concepto.de/solucion-quimica/

Deixa un comentari