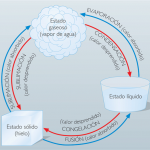
En física i química s’anomena canvi d’estat a l’evolució de la matèria entre diversos estats sense que hi hagi canvis en la seva composició. Els tres estats bàsics són el sòlid, el líquid i el gasós, a aquests tres cal afegir l’estat de plasma.
La següent taula indica com s’anomenen els canvis d’estat.
| Inicial\Final | Sòlid | Líquid | Gasós | Plasmàtic |
|---|---|---|---|---|
| Sòlid | Fusió | Sublimació o sublimació progressiva | ||
| Líquid | Solidificació | Evaporació i ebullició | ||
| Gasós | Sublimació inversa o regressiva | Condensació i liquació | Ionització | |
| Plasmàtic | Recombinació/Desionització |
Els dos paràmetres dels que depen que una substància o mescla es trobi en un estat o en un altre són la temperatura i la pressió.
Diferència entre evaporació i ebullició
Els líquids poden canviar a vapor a una temperatura per sota els seus punts d’ebullició a través del procés d’evaporació. L’evaporació és un fenomen superficial en el qual les molècules situades a prop de la superfície vapor/líquid s’escapen cap a la fase vapor. Per altra banda, l’ebullició és un procés en el qual les molècules s’escapen de qualsevol part del líquid, com a resultat de la formació de bombollles de vapor dins del líquid.