L’atmosfera és l’embolcall extern de la Terra format per la mescla de gasos anomenada aire i que està lligat a la Terra gràcies a la força de la gravetat. El límit superior es considera 10000km, malgrat que en aquest punt la densitat de l’aire és baixíssima. La presència de l’atmosfera és imprescindible per a la vida actual i, tal i com es veurà més endavant, l’evolució de la composició de l’atmosfera i l’evolució de la vida estan estretament lligades
Evolució de l’atmosfera
La composició de l’atmosfera no ha estat constant durant la història de la Terra, per tant, abans d’explicar-ne la composició actual, val la pena repassar com s’ha arribat fins a l’estadi actual. L’atmosfera original (o primitiva) derivava dels gasos originals procedents de la nebulosa solar a partir de la qual es va formar el Sistema Solar i de la desgasificació interna (erupcions volcàniques). Aquesta atmosfera estava formada per N2, CO2, HCl, SO2, H2O, He i H (aquests dos últims es van perdre perquè no van poder ser retinguts per la gravetat). Més tard el vapor d’aigua va començar a condensar per la baixada de la temperatura (fa uns 4000Ma) i es van produir les primeres precipitacions, i l’acumulació d’aquestes va permetre la formació dels oceans.
En aquest context d’atmosfera reductora, en els oceans es va originar la vida. Els primers éssers vius en colonitzar el planeta van ser els bacteris anaeròbics i les cianobactèries (aquestes últimes són fotosintètiques). Al principi l’O2 produït era consumit per a oxidar els elements i compostos presents en l’oceà, ja que el O2 seguiria dissolt en l’aigua. Fa aproximadament 2000Ma, l’aigua dels oceans es va saturar en O2 i aquest es va alliberar a l’atmosfera, convertint-la en oxidant i permetent que es formés ozó (O3) i per tant fent que l’atmosfera adquirís una composició favorable per a la colonització dels continents.
Composició
L’atmosfera és una barreja de gasos i aerosols (petites partícules líquides i sòlides disperses). Aquesta barreja no és homogènia en tota la seva potència i per això es divideix en zones segons la composició: homosfera (primers 90km) i heterosfera (la resta). A més, aquestes dues zones es poden dividir en estrats segons el seu comportament.
La composició de l’homosfera es considera en sec, és a dir, sense tenir en compte la proporció de vapor d’aigua, ja que és molt variable. Els principals gasos presents són N2 (78,1%), O2 (21,0%), Ar (0,9%), CO2 (0,03%) i en menors proporcions Ne, He, CH4, Kr, H, Xe, O3, NO, NH3….
Inicialment però aquestes proporcions no eren així. Gràcies a l’anàlisi del registre geològic se sap que el percentatge de CO2 ha anat disminuint exponencialment des de fa 4500Ma, el de N2 ha augmentat (mantenint-se constant en els últims 2000Ma) i l’O2 ha augmentat el seu percentatge progressivament des de que va aparèixer fa 2000Ma.
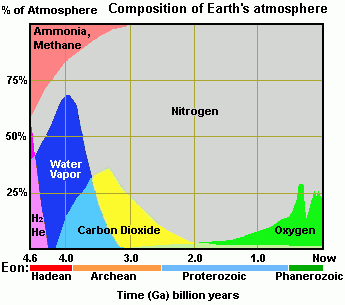 Figura: composició de l’atmosfera al llarg del temps. Extret de: web (autor de la figura desconegut)
Figura: composició de l’atmosfera al llarg del temps. Extret de: web (autor de la figura desconegut)
Val la pena mencionar el cas del O3, ja que la majoria es troba concentrat en al capa d’ozó a 20-35 km d’altitud. L’ozó és el producte de la reacció d’O2 i radiació ultraviolada. Les molècules que es formen justament impedeixen que una gran part d’aquesta radiació arribi a la superfície terrestre. Curiosament, aquest gas en altituds baixes és tòxic.
L’heterosfera està formada per 4 capes des del punt de vista de la seva composició química amb límits difusos:
- 90-200km: N2
- 200-1100Km O (atòmic)
- 1100-3500: He
- >3500 fins on la densitat d’H és la mateixa que en l’espai interplanetari
Estructura
Tal i com s’ha dit, l’homosfera i l’heterosfera es divideixen en capes segons el seu comportament físic. Les zones de transició entre els estrats s’anomenen pauses:
- Troposfera: és la capa inferior, és a dir, la que està en contacte amb la superfície terrestre. Té un gruix variable (17km a l’Equador, i 8km als pols) i la seva presència és clau en el desenvolupament de la vida i en la geodinàmica externa, ja que és la capa on es produeixen els fenòmens meteorològics (que a la vegada condicionen les zones climàtiques de la Terra). En aquesta capa, la temperatura de l’aire disminueix des de la superfície fins a la troposausa (-50ºC) amb un gradient d’1ºC/150m. Les masses d’aire es mouen verticalment per convecció tèrmica, ja que les parts baixes reben la calor emesa des de l’interior de la Terra.
- Estratosfera: Té el límit superior a 50km d’altitud i inclou la capa d’ozó (aquesta darrera no té una distribució homogènia, sinó que en els pols és més prima). En l’estratosfera la temperatura torna a augmentar, primer a poc a poc (fins als 30km) i després amb un gradient major fins a assolir els 80ºC. Els desplaçaments d’aire són en horitzontal.
- Mesosfera: passada l’estratopausa hi ha la mesosfera que arriba fins a uns 80km i on la temperatura disminueix fins als -100ºC. El límit superior (la mesopausa) coincideix amb el límit superior de l’homosfera
- Termosfera: el seu límit inferior coincideix amb el de l’heterosfera. Està caracteritzada perquè els valors de temperatura tornen a ser creixents amb l’altitud fins als 1100-1600ºC a causa de la ionització dels gasos. De fet s’anomena ionosfera a aquesta zona d’alta ionització, a vegades fins i tot usant el mot com a sinònim de termosfera i es divideix en més subcapes i regions (de baixa a alta altitud: regió D, capa D, regió E, capes F1 i F2, regió F). Arriba fins als 600-800km.
- Exosfera: per damunt la termopausa es troba la capa on la densitat de l’aire és molt baixa fins a igualar-se a la de l’atmosfera solar, principalment hi ha He i H i arriba fins als 10000km.
- Magnetosfera: és la regió al voltant de la Terra on, malgrat ja no hi ha aire, el camp magnètic hi actua com a escut, modificant o organitzant les partícules d’alta energia procedents del Sol.
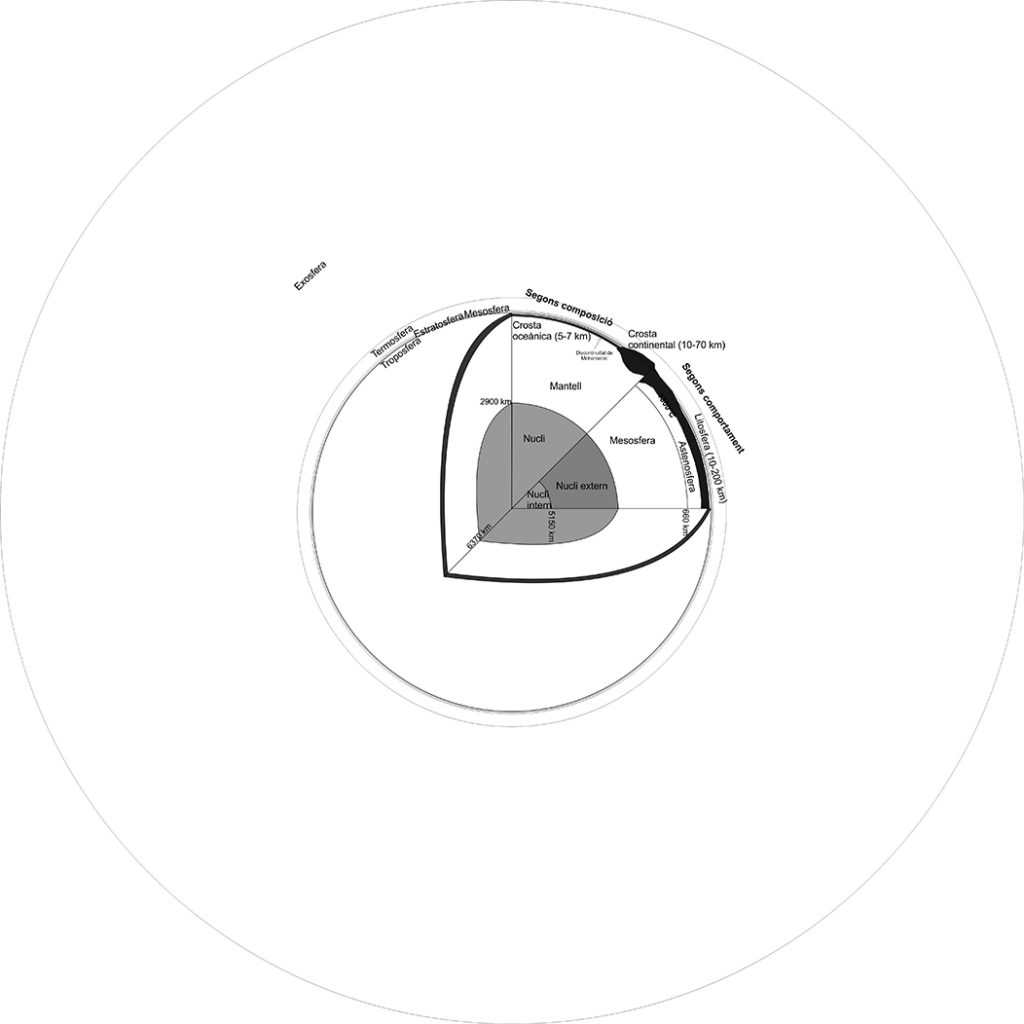 Figura original. Capes de l’atmosfera a escala i en relació amb les capes internes
Figura original. Capes de l’atmosfera a escala i en relació amb les capes internes
Dinàmica de l’atmosfera
En la troposfera s’hi produeixen els fenòmens meteorològics que afecten al desenvolupament de la vida i als processos relacionats amb la geodinàmica externa. A continuació es descriuen ens principals factors meteorològics:
- Temperatura de l’aire: és la magnitud que mesura l’energia tèrmica. Les fonts d’energia tèrmica són el Sol i l’interior de la Terra. En el primer cas, l’energia depèn de l’angle d’incidència del Sol i de la quantitat d’hores d’exposició. Així la temperatura de l’atmosfera depèn de la latitud i del dia de l’any. La temperatura de les masses d’aire té un paper clau en el seu moviment, ja que a majors temperatures la densitat baixa i les masses tendeixen a ascendir.
- Pressió atmosfèrica: la pressió és el pes de la columna d’aire que gravita sobre un determinat element unitari de superfície i es mesura amb el baròmetre. Al nivell del mar la pressió atmosfèrica és d’1kg/1cm3 i disminueix amb l’altitud. Aquest valor varia per culpa de la temperatura de l’aire. Si la pressió és major que la calor normal esperada, la zona és un anticicló (masses d’aire fred), mentre que si és menor és una depressió (masses d’aire calent). Les línies que uneixen els punts d’igual pressió s’anomenen isòbares. En l’interior de les depressions l’aire calent ascendeix mentre que en els anticiclons l’aire fred baixa. Teòricament, tenint en compte que la temperatura de l’aire és major a l’equador que als pols, s’haurien de produir una circulació d’aire des dels pols fins a l’equador. Aquest model no funciona, ja que la inclinació de l’eix de rotació i la pròpia rotació produeix l’efecte Coriolis que es tradueix en un total de 6 cèl·lules convectives (de nord a sud): a) anticicló al pol nord, b) depressió a uns 60ºN, c) anticicló a uns 30ºN, d) depressió a l’equador, e) anticicló a 30ºS, f) depressió a 60ºS i g) anticicló al pol sud.
- Humitat atmosfèrica: és la magnitud que mesura la quantitat de vapor d’aigua. La quantitat que n’admet l’aire és depenent de la temperatura d’aquest, a més temperatura més vapor d’aigua admet. Es distingeix entre humitat absoluta, que és els grams d’aigua per metre cúbic d’aire, i la relativa, que és el percentatge respecte la humitat total que pot contenir l’aire a una temperatura concreta abans de condensar. L’aparell que mesura la humitat relativa s’anomena higròmetre
- Precipitació: és la caiguda des de l’atmosfera cap a la superfície de la Terra d’aigua en estat líquid o sòlid. Quan les masses d’aire arriben a una humitat relativa del 100% (punt de saturació), el vapor d’aigua es condensa formant núvols o boira (cal remarcar que per a que això es doni han d’existir nuclis de condensació, que poden ser partícules en suspensió, pol·len, aerosols, etc). La humitat relativa puja quan la temperatura baixa. Segons el context al que s’associï l’augment de la humitat relativa es distingeixen pluges: a) a les depressions, on l’aire calent i humit ascendeix i es refreda, b) orogràfiques si l’ascensió es produeix per culpa de l presència d’un relleu positiu, i c) anticiclòniques, si xoquen dues masses d’aire diferents, on la calenta i menys densa passa per damunt i a més altitud es refreda. També existeix la pluja amagada que és la condensació del valor d’aigua amb el sòl fred i que forma rosada o gebrada.
- Vent: és aire en moviment amb el sentit d’anticiclons cap a depressions seguint el gradient isobàric (en vent va de les altes a les baixes pressions). La direcció que pren el vent no és perfectament perpendicular a les isòbares, i és obliqua per culpa de l’efecte Coriolis. El vent juga un paper fonamental en el desplaçament de les masses d’aire a diferents temperatures.
Contaminació atmosfèrica
La contaminació és l’augment de substàncies perjudicials o certes formes d’energia (calor, soroll, radioactivitat) en el medi ambient, en aquest cas l’atmosfera, en quantitats més altes de les que el medi és capaç de neutralitzar. La contaminació pot ser deguda a processos naturals, per exemple erupcions volcàniques, o per activitat humana. En aquest darrer cas el focus pot ser fix o mòbil.
Principals substàncies químiques contaminants: existeixen dos tipus de contaminants segons si són abocats directament a l’atmosfera (contaminant primari) o si es produeixen com a conseqüència de transformacions químiques i fotoquímiques (contaminants secundaris). En el primer cas hi ha aerosols sòlids o líquids i gasos com el SO2, SO3, H2S, NO, NO3, CO, CO2, metalls pesants (Pb, Cr, Cu, Mn, V, Ni, As, Cd, Hg), minerals com l’asbest o l’amiant, compostos hal·logenats i els seus derivats (HCl, Cl2), compostos orgànics (hidrocarburs aromàtics, mercaptans, dioxines, furans), substàncies radioactives, bactèries i pol·len. En el segon cas es produeixen: a) oxidants en reaccionar entre sí els òxids de nitrogen, els hidrocarburs i l’O2 en presència de radiació ultravioleta; b) àcid sulfúric per la reacció dels òxids amb l’aigua; o c) es destrueixen molècules d’ozó per la reacció d’aquestes amb CFC (cluorofluorocarburs)
Factors a tenir en compte: les condicions atmosfèriques, meteorològiques i climàtiques tenen un paper important en el grau de contaminació, ja que poden arribar a dificultar la neutralització dels contaminants. Un exemple quotidià són els episodis de contaminació atmosfèrica anomenat SMOG que succeeixen quan les partícules en suspensió al voltant d’una gran ciutat no es dispersen per culpa de la presència d’un anticicló
Efectes de la contaminació, locals o globals: Dins dels efectes locals s’inclouen totes aquelles malalties i afectacions en l’aparell respiratori dels éssers vius, els relacionats amb la contaminació radioactiva i la pluja àcida. La pluja àcida és la precipitació d’aigua amb un pH molt baix causat per la dissolució d’àcid sulfúric en les gotes de pluja. Els òxids de sofre i nitrogen que causen la pluja àcida són emesos per zones industrials no gaire allunyades d’on s’acaba produint la precipitació. La pluja àcida afecta la massa arbòria i la resta de plantes, però també edificis i altres materials antròpics exposats
Els efectes globals més coneguts són l’efecte hivernacle i la destrucció de la capa d’ozó. L’efecte hivernacle és l’augment de la temperatura mitjana del planeta causada per l’emissió de CO2, H2O, CH4, òxid nitrós (N2O), etc. Aquests gasos es disposen en l’atmosfera en una capa que permet que la radiació solar penetri fins a la superfície terrestre, però no que després pugui rebotar i retornar a l’espai, sinó que es torna a reflexar en la superfície.
La disminució de la capa d’ozó està causada per la reacció entre els CFC i les molècules d’ozó. En aprimar-se aquesta capa, la capacitat de retenir la radiació ultraviolada baixa i per tant aquesta arriba a la superfície terrestre i afecta als éssers vius, causant per exemple càncer de pell.
L’últim efecte global és l’acumulació de substàncies tòxiques en les cadenes tròfiques, ja que els contaminants orgànics no degradables (ex. insecticida DDT) romanen en el medi, incorporant-se en els teixits i després a les cadenes tròfiques
Mètodes de determinació i correcció
Per a determinar la qualitat de l’aire es mostreja seguint diferents criteris: a les proximitats dels possibles focus, o dels elements vulnerables, o en àrees aleatòries o de forma puntual o prolongada i sistemàtica en el temps. S’usen col·lectors, que són diferents segons el component d’interès. Alguns són d’absorció, filtres impregnats amb radioactius, tubs de difusió, adsorció o condensació.
La Xarxa de Vigilància i Previsió de la Contaminació Atmosfèrica forma part del Departament de Territori i Sostenibilitat de la Generalitat de Catalunya i el seu objectiu és detectar els nivells dels principals contaminants, i té associats diferents punts de mostreig (automàtics o manuals) que permeten definir zones de qualitat de l’aire.
Les mesures de correcció dels contaminants són dues: retenir i controlar els contaminants, o disminuir-ne la seva producció. Evidentment aquesta darrera solució és la desitjada i és cap on es dirigeixen els acords assolits a l’Acord de París dins del Conveni Marc de les Nacions Unides sobre el Canvi Climàtic (12/12/2015), que malauradament no està sent posat en pràctica per molts països
Una de les darreres novetats a Catalunya que s’ha començat a implementar el 1/12/2017 és que els turismes no podran circular dins de la zona de baixes emissions de l’àrea metropolitana en episodis de contaminació. Per tal d’identificar aquests vehicles, s’hauran de dur etiquetes amb les seves característiques (A-C, juntament amb colors).
La correcció depèn de tots i no serà efectiva fins que els interessos econòmics deixin de prevaldre per davant dels ambientals.


 (
(
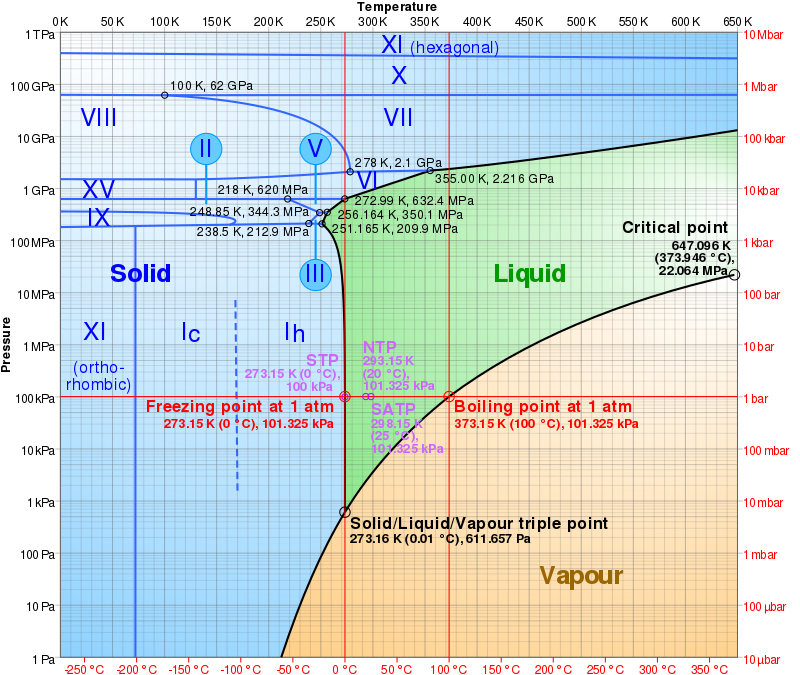 Diagrama de fases de l’aigua. Extret de Cmglee (2018)
Diagrama de fases de l’aigua. Extret de Cmglee (2018) 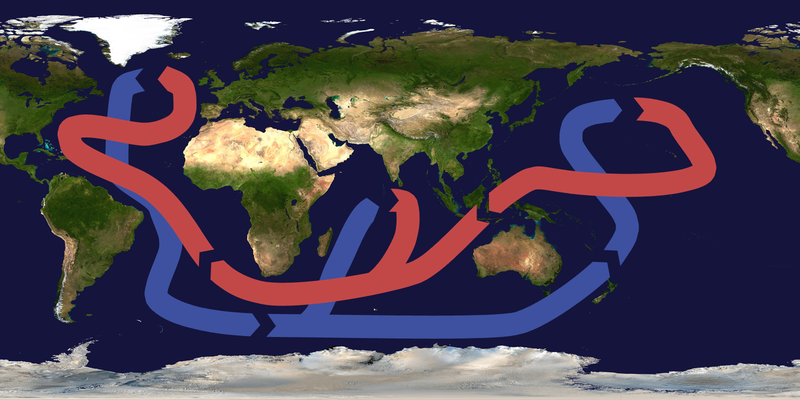 Circulació termohialina. Extret de Brisbane (2009)
Circulació termohialina. Extret de Brisbane (2009) 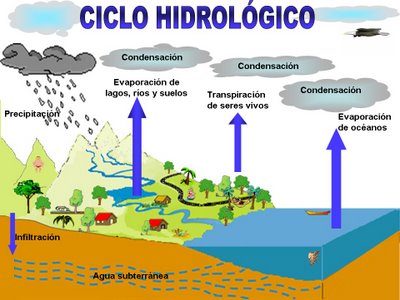 Cicle hidrològic. Extret de
Cicle hidrològic. Extret de 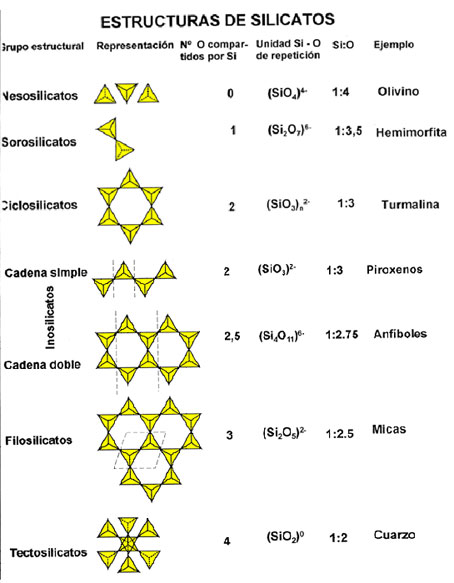 Estructura dels grups de minerals silicatats. Extret de:
Estructura dels grups de minerals silicatats. Extret de:  Figura: composició de l’atmosfera al llarg del temps. Extret de:
Figura: composició de l’atmosfera al llarg del temps. Extret de:  Figura original. Capes de l’atmosfera a escala i en relació amb les capes internes
Figura original. Capes de l’atmosfera a escala i en relació amb les capes internes