Dijous 12 de setembre del 2019; tutoria 1rD
https://forms.gle/Pd3G3zwTkNT7iEyr5

20190505
Aquesta setmana…
…el papa ha començat a treballar. Què vol dir això? Això vol dir que has hagut de passar moltes hores a soles amb mi, una situació temuda des del primer dia que et vaig tenir en braços: I si faig una cosa malament? I si no arribo a tot? I si no soc capaç de saber què et passa quan plores? I si em sento molt sola?
La veritat és que puc dir que no ha estat tan terrible com em pensava (sobretot perquè hem rebut companyia i ajuda de la tieta). Sí, ho reconec, les coses van més lentes i a vegades no es pot fer tot el que una vol (l’evidència és el retard amb el que surt l’escrit d’aquesta setmana), però ens hem organitzat, i fins i tot hem agafat per primer cop el tren per anar a Barcelona! Aquests dies també m’han servit per a fer una reflexió i valorar encara més les cinc setmanes que hem compartit inicialment tots tres (sobretot les dues primeres durant les quals jo encara em trobava tant malament i dèbil).
El dia 22 de febrer vam anar a mirar roques en façanes amb els estudiants de 1r de Batxillerat.
L’explicació de l’excursió es pot trobar al següent enllaç
La hidrosfera és el conjunt de totes les aigües que formen el segon embolcall fluid de la Terra i les aigües superficials (mars, llacs, rius, glaceres, neu, etc). En el diccionari de geologia d’Oriol Riba (1997), no s’especifica si també s’han de considerar les aigües subterrànies i l’aigua present en l’atmosfera que es troba en estat gas (aquesta també forma part del cicle de l’aigua), però aquí s’hi consideren.
La coexistència a temperatura ambient d’aigua en els tres estats (sòlid, líquid i gas) és possible gràcies al fet que les condicions de pressió i temperatura mitjanes a la superfície de la Terra són molt properes al punt triple de l’aigua (0,006 atm, i 0,01ºC). Això no sempre ha estat així. En els primers estadis de formació de la Terra no hi havia aigua líquida degut a les altes temperatures a les que es trobava la Terra. Aleshores, l’aigua es trobava en l’atmosfera en forma de gas i provenia de la desgasificació de la Terra gràcies als volcans i dels meteorits i asteroides que hi van impactar de forma tardana. En anar disminuint la temperatura de la superfície, l’aigua es va condensar i es van formar els grans reservoris d’aigua.
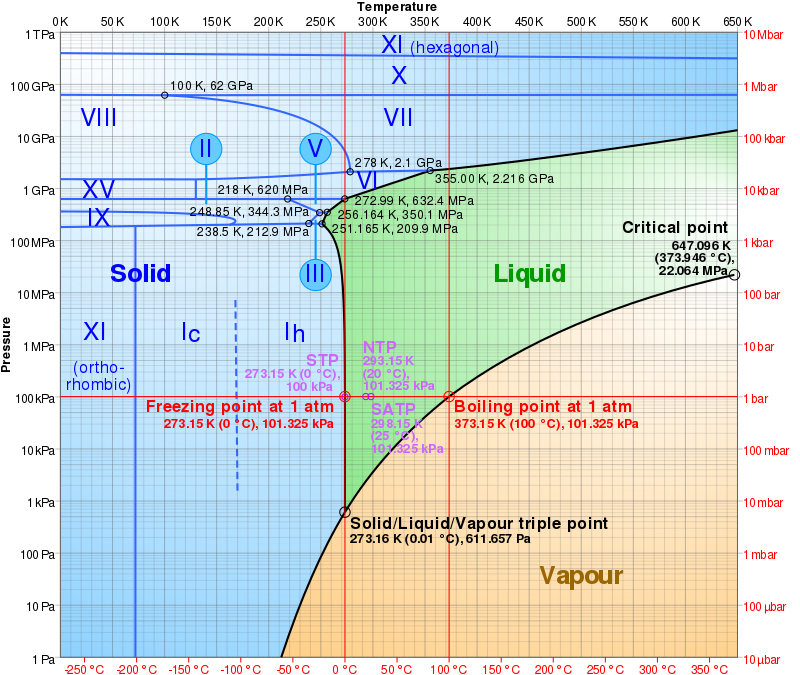 Diagrama de fases de l’aigua. Extret de Cmglee (2018) link
Diagrama de fases de l’aigua. Extret de Cmglee (2018) link
Distribució de l’aigua a la Terra
La hidrosfera cobreix ⅔ parts de la superfície de la Terra, principalment en els oceans (97,2%), però també és present en forma de gel glaceres (2,15%), aigües subterrànies (0,62%), rius i llacs (0,017%), vapor d’aigua en l’atmosfera (0,001%) i formant part dels éssers vius (0,0005%). És a dir, es troba en els 3 estats.
Composició i característiques físiques de l’aigua
L’aigua és la molècula H2O, però en la natura no s’acostuma a trobar en estat pur, sinó que acompanyant-la, en dissolució s’hi troben sals, gasos i partícules en suspensió. Un exemple són els oceans on, en dissolució, s’hi troben quasi tots els elements químics (tot i que la majoria en quantitats inapreciables, de fet només 6 dels elements configuren el 99% dels ions dissolts en les aigues marines). S’anomena salinitat a la quantitat de sals en dissolució, que és molt més elevada en oceans que en les aigües continentals.
En general, la solubilitat de les sals augmenta amb la temperatura i per tant com més calenta estigui l’aigua més sals hi haurà dissoltes. Això no passa amb els gasos, que tenen un comportament diferent (es dissolen millor en general a baixes temperatures). Tampoc segueix la norma general el carbonat de calci. Aquest compost és més soluble en aigua freda (també influenciada pel pH de l’aigua).
Les diferències de densitat de les diferents masses d’aigua (depenents de la temperatura i la salinitat) tenen un paper clau en l’estratificació de les aigües i en la circulació d’aquesta (coneguda amb el nom de circulació termohialina). La circulació de les aigües oceàniques també està condicionada per la distribució dels continents que contribueix a la zonificació climàtica del planeta, que regula la temperatura.
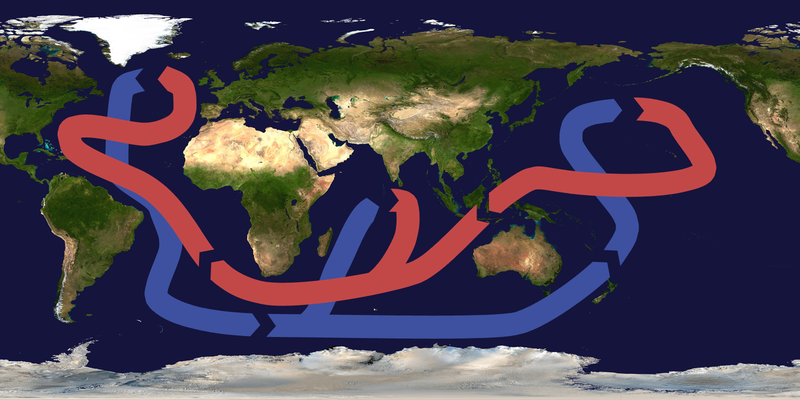 Circulació termohialina. Extret de Brisbane (2009) link
Circulació termohialina. Extret de Brisbane (2009) link
Altres característiques físiques que cal tenir en compte són l’acidesa del medi i la terbolesa (determina fins a quina profunditat penetra la radiació solar visible, és a dir, la llum). Pel que fa a la terbolesa, es distingeixen dues zones, la zona fòtica que és on arriba la llum i hi pot tenir lloc la fotosíntesi, i la zona afòtica, on no hi arriba llum. Segons la terbolesa, la zona fòtica arriba fins a una profunditat o una altra, i varia de pocs centímetres a 200m.
El cicle de l’aigua
El cicle de l’aigua no té principi ni fi, però per a explicar-lo es pot començar per l’evaporació que es produeix tant d’aigües oceàniques com continentals quan l’aigua s’escalfa i passa a estat gas. Un cop a l’atmosfera i per culpa del refredament, es condensa en forma de pluja o solidifica en forma de neu o pedra. Amb les condicions adequades, es produeixen les precipitacions, que un cop arriben en superfície poden prendre tres camins: a) filtrar-se i incorporar-se a un aqüífer, b) quedar retingudes per la vegetació o altres éssers vius, o c) escolar-se per la superfície terrestre. Aquests tres camins porten a l’equació del balaç hídric (una equació que iguala les entrades i les sortides d’aigua per a que pugui seguir el cicle):
Precipitacions = Escolament Superficial + Infiltració + EvoTranspiració
Tant en el cas de l’aigua infiltrada com la d’escolament, aquesta tendeix a desplaçar-se (en superfície o en el subsòl) seguint el gradient piezomètric en direcció a l’oceà on el valor de l’altura piezomètrica és zero. Pot donar-se el cas que l’aigua de l’escolament s’evapori o s’infiltri abans d’arribar a l’oceà, i que la infiltrada sigui aprofitada pels éssers vius. Els éssers vius perden aigua per transpiració en un procés anomenat evotranspiració.
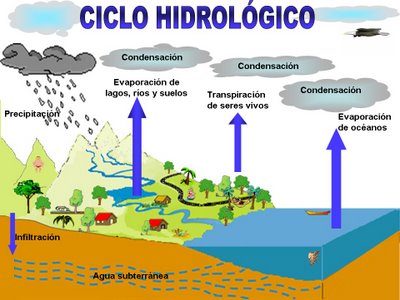 Cicle hidrològic. Extret de link
Cicle hidrològic. Extret de link
Contaminació de l’aigua i els seus impactes
La contaminació és l’augment de substàncies perjudicials o d’algunes formes d’energia (calor, radioactivitat) en el medi ambient, en el cas que ens ocupa l’aigua, en quantitats més altes de les que el medi és capaç de neutralitzar. Aquesta contaminació pot ser natural o antròpica.
Els agents contaminants de l’aigua són variats i per tant poden tenir diferents conseqüències en el medi i per tant en els éssers vius. A continuació es presenten alguns contaminants segons la seva naturalesa:
Les principals fonts de contaminació antròpiques són les industrials, les urbanes o agrícoles, que poden tenir un caràcter puntual o difús, i poden afectar qualsevol medi aquàtic. La morfologia del contaminant en aigües subterrànies amb un origen puntual és a grans trets un plomall on la concentració a les proximitats de la font és més alta i va disminuint a mida que se n’allunya, mentre n’augmenta el volum de roca contaminat. És important no entendre cada medi aqüàtic de forma aïllada, ja que estan tots interconnectats, tal i com s’ha vist en l’apartat del cicle de l’aigua. Per tant, un contaminant en el subsòl pot passar a aigües superficials i al revés.
Alguns dels impactes de la contaminació de l’aigua són:
Depuració, potabilització i descontaminació
La potabilització és el conjunt de processos que transformen les aigües naturals en aigües aptes per a l’ús humà (característiques físiques, químiques i biològiques que no representin un risc per a la salut). El tractament que es fa a les aigües naturals dependrà del seu estat original i de l’ús que se’n vulgui fer. Per a potabilitzar l’aigua es filtren els sòlids, es deixa que les partícules en suspensió decantin i s’hi afegeix clor per a desinfectar-la.
La depuració és el tractament al qual se sotmeten les aigües residuals procedents de zones agrícoles, poblacions, indústries, etc… després d’usar-les perquè recobrin les seves propietats naturals abans de retornar-les a la natura. Aquest procés es duu a terme en les centrals depuradores. Inicialment s’hi fa una depuració física, que inclou un pretractament per a eliminar les partícules grolleres, els olis i greixos i una decantació per a eliminar els fangs primaris. Després s’hi realitza una depuració biològica per a eliminar la contaminació orgànica, on hi ha una desinfecció per clor o radiació ultravioleta.
Per a descontaminar el medi aquàtic en primer lloc s’ha de fer un anàlisi de qualitat de les aigües en qüestió. Una vegada fet aquest, cal aïllar la font i després aplicar el mètode corresponent segons el contaminant. La principal diferència entre descontaminar una massa d’aigua en superfície o en el subsòl és el mostreig i el monitoreig del procés, ja que en el segon cas s’ha de fer amb pous i sondatges. Alguns dels mètodes de descontaminació de les aigües subterrànies són: a) tractament amb co-solvents (injectant-los si és en un aqüífer) que són substàncies per tractar els compostos orgànics immiscibles, b) tractament amb tensioactius, que faciliten descontaminar els hidrocarburs (són molt tòxics); c) injecció de substàncies amb alt poder oxidant/o reductor segons el que calgui; d) afegint organismes que puguin biodegradar el contaminant; e) filtrant mecànicament les partícules més grans; f) adsorvint el carboni que elimina la matèria orgànica dissolta; i g) per intercanvi iònic.
El problema de la manca d’aigua
L’aigua com a recurs es pot definir com a renovable o com a no renovable al mateix temps. D’una o altra definició depèn la zona del planeta a on es faci referència (amb un clima concret) i del tipus d’ús que se’n vulgui fer. A més a més, el canvi climàtic actual està provocant modificacions importants en el règim, distribució (temporal i espaial) i característiques de les pluges.
El problema de la manca d’aigua doncs apareix quan es trenca l’equilibri hídric i la demanda i ús d’aigua potable són superiors a la seva disponibilitat. És en aquest moment quan es passa a dir que el recurs és no renovable. És responsabilitat dels humans adaptar l’ús a la disponibilitat. Això es pot aconseguir amb accions quotidianes, com ara usar cisternes del lavabo amb doble càrrega, o fent un bon manteniment de canonades i aixetes, evitant banyeres i sense abusar de les activitats lúdiques.
Hom podria argumentar que hi ha molta aigua disponible al mar, però aquesta, degut a les seves característiques de salinitat, no pot ser usada directament, sinó que primerament se li ha de fer un tractament en plantes dessalinitzadores. Aquest tractament és costós energèticament (i per tant també econòmicament) i per tant és recurs que només s’usa en casos d’extrema sequera quan els embassaments estan a unes reserves molt baixes (<25% de capacitat), com és el cas de finals de novembre del 2017 i desembre on les plantes desalinitzadores produien set vegades més aigua dolça que en una situació normal.
Així doncs, per fer un ús responsable cal remuntar-se a l’apartat del cicle de l’aigua i prendre consciència que només es pot usar l’aigua existent en el sistema. Algunes propostes realitzades per alguns governs justament trenquen aquest equilibri, com pot ser el Plan Hidrológico Nacional on, per abastar zones on s’havia augmentat la demanda d’oci de forma artificial, s’estava disposat a trencar l’equilibri natural que funcionava en altres zones.
Comparteixo un article del dia 18 de setembre publicat pel Royal Tyrrel Museum de Canadà. En aquest article es fa un bon resum divulgatiu (en anglès, això sí) sobre la fossilització. Amb l’ajuda de fotografies permet començar a entendre què són els fòssils i gràcies a quins processos s’han format
Sovint no pensem que els terratrèmols són perillosos. I no ens equivoquem. Però el que encara són més perilloses són els fenòmens geològics que poden desencadenar. Un dels més habituals són els moviments de massa.
En aquestes imatges publicades a Facebook per “The Next California Earthquake” el dia 6 de setembre del 2018, es pot observar la quantitat d’esllavissades ocorregudes durant l’esdeveniment del 5 de setembre del 2018 a Hokkaido (M6,6).


Els minerals són un dels components de les roques, juntament amb, per exemple, els fòssils, la porositat o altres fragments de roques. En el cas de les roques metamòrfiques en són l’únic component.
Un mineral és un producte natural, sòlid, inorgànic i d’estructura cristal·lina i composició química definida. Tenint en compte aquesta definició: un diamant artificial, el petroli i l’òpal no són minerals.
Una roca per la seva part és un material d’origen natural, en estat sòlid, i formada per un o més minerals i opcionalment altres components formadors de roques no minerals (fòssils, porositat, vidre, fragments de roca, fluids, clasts, ciment i components orgànics) que presenta una homogeneïtat estadística (en detall no, ja que pot ser heterogènia).
Es coneixen gairebé 4000 minerals i cada any se n’identifiquen de nous. La majoria d’ells estan formats per vuit elements, que són els 8 elements que representen més del 98% en pes de l’escorça continental. Aquests elements són per ordre d’abundància: oxigen (46,6%), silici (27,7%), alumini (8,1%), ferro (5%), calci (3,6%), sodi (2,8%), potassi (2,6%) i magnesi (2,1%).
Classificació composicional dels minerals
Tal i com s’ha vist en l’apartat anterior, els dos elements més abundants en l’escorça són l’oxigen i el silici. Aquests dos elements tendeixen a combinar-se per a formar l’estructura del grup mineral més comú, els silicats, i que representa el 90% de l’escorça terrestre. És tant gran aquesta abundància respecte la resta de grups que la classificació dels minerals es pot dividir en silicats i en no silicats.
(degut a la manca de fotografies pròpies de tots aquests minerals, copio dos enllaços per a poder consultar les fotografies de tots els que es mencionen en aquesta entrada del blog: el primer és una galeria de minerals especialitzada en els minerals de Catalunya, i el segon és una col·lecció del 2008 on es poden consultar per nom)
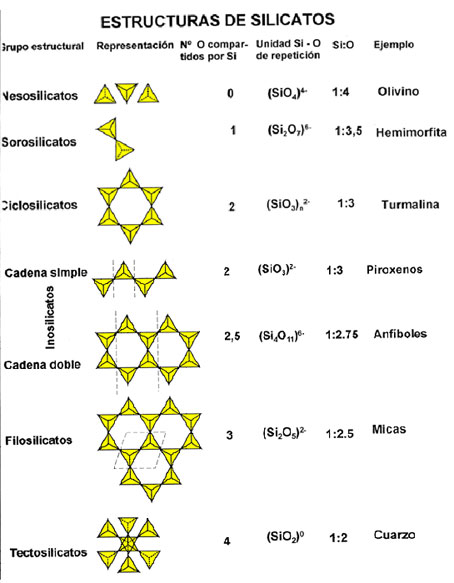 Estructura dels grups de minerals silicatats. Extret de: enllaç
Estructura dels grups de minerals silicatats. Extret de: enllaç
Classificació genètica
La gran varietat composicional i estructural dels minerals resulta en condicions concretes de cristal·lització. A continuació es classifiquen segons el seu ambient de formació:
Fluids hidrotermals, associats a aigües residuals magmàtiques. En aquests casos destaca la formació d’òxids (hematites) i sulfurs (cinabri, magnetita, esfalerita, galena, pirrotita, calcopirita, i pirita)
Usos dels minerals
En aquesta taula es poden observar alguns dels usos de minerals:
| Mineral | Element que se n’extreu | Objectes i substàncies on s’emplea |
| Atzurita | Coure (Cu) | Pigment blau (pintures), joieria |
| Barita | Bari (Ba) | Pintura blanca, color verd dels focs artificials |
| Calcita | Calci (Ca) | Ciment, antiàcid (medicina), pasta de dents, maquillatge en pols |
| Calcopirita | Coure (Cu) | Peces de llautó (instruments de metall) o de bronze (campanes, monedes), cables |
| Cinabri | Mercuri (Hg) | Termòmetre analògic, làmpades fluorescents |
| Esfalerita | Zinc (Zn) | Peces de llautó (instruments de metall), desodorants, cremes solars |
| Fluorita | Fluor (F) | Tefló de les paelles, Gore-Tex, antidepressiu (medicina) |
| Galena | Plom (Pb) | Bateries, canonades |
| Guix | Revestiment de parets, embenats (medicina) | |
| Halita | Sodi (Na) | Sal de cuina |
| Hematites | Ferro (Fe) | Cotxes, eines, estructures, purpurina, pigment vermell (pintures) |
| Magnetita | Ferro (Fe) | Cotxes, eines, estructures, llimes d’ungles |
| Malaquita | Coure (Cu) | Pigment verd (pintures) |
| Moscovita | Pastilles de fre (aïllant), extintor en pols, maquillatge, pintures d’ungles | |
| Ortosa | Vidre, porcellana de lavabo, cautxú | |
| Pirolusita | Manganés (Mn) | Llaunes de refresc, piles alcalines, pigment negre (pintures) |
| Quars | Silici (Si) | Microxips, vidre, silicona, pasta de dents, paper de vidre |
| Silvina | Potassi (K) | Fertilitzant, pólvora |
| Sofre | Sobre (S) | Pesticida, cautxú |
| Talc | Cautxú, blanquejant, pólvores de talc, pastilles (medicina), llaminadures | |
| Wolframita | Tungstè (W) | Filaments bombetes tradicionals, punta de bolígrafs, broques i eines de tall |
Sempre va bé tenir-la a mà!
Aquest estiu s’ha actualitzat. En aquest enllaç s’hi pot trobar la versió en anglès. També es pot accedir a la versió catalana, tot i que no està actualitzada
En aquesta imatge es pot comprovar que a Catalunya compartim zona horària amb països com ara Albània.
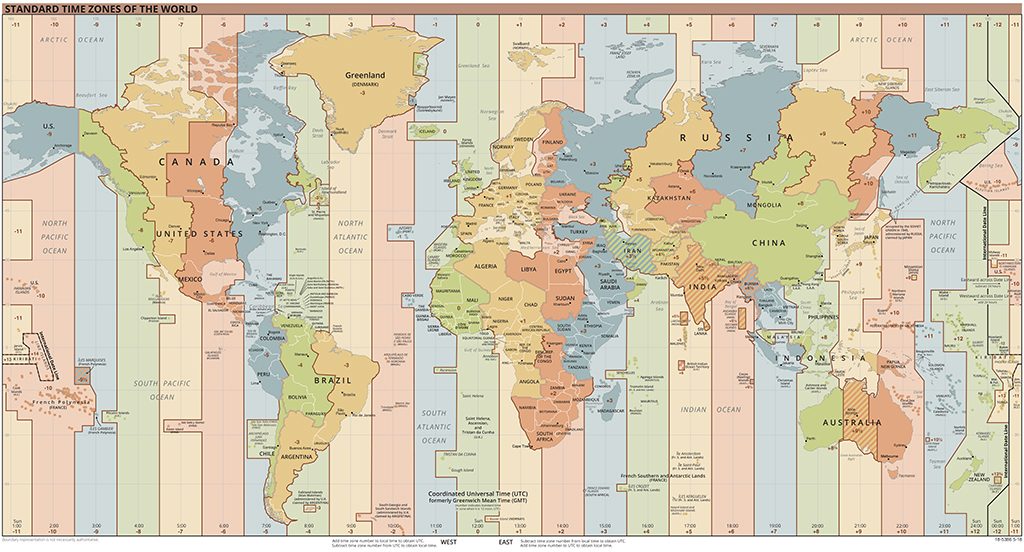 Zones horàries estàndard del món; extret de: Link, domini públic)
Zones horàries estàndard del món; extret de: Link, domini públic)
No tinc res en contra Albània. Però agafo aquest país d’exemple perquè la seva capital (Tirana) es troba a una latitud (41º20’N) molt semblant a la de Barcelona (41º22’N) i, per tant, em va molt bé per a comparar qualsevol dia de l’any (no necessàriament durant els equinoccis, on tots els punts de la Terra gaudeixen de les mateixes hores de llum).
Resulta que, tot i compartir latitud, amb els habitants de Tirana ens separen 17º39′ de longitud. Aquesta diferència és la responsable que avui, dia 31/08, a Tirana la sortida del sol hagi ocorregut a les 06:06 i a Barcelona una hora i deu minuts més tard (07:16). Igualment passarà amb la posta de sol, entre les 19:15h i les 20:26h.
O ens emmarquem en la zona horària que toca per longitud (i no per relacions històriques), o deixem de pretendre compartir costums horaris i acceptem la nostra vida lligada a la llum!!!