PROGRAMACIÓ D’AULA.
CURS D’ACCÈS CAS 2014-2015
PROGRAMA QUIMICA-BIOLOGIA OFICIAL
Temari_cas_quimica_biologia
(proposat pel Departament d’Ensenyament)
- S’adaptarà al curs donada l’amplitud de continguts que hi ha i del poc temps que es disposa.
- El contingut total es distribuirà així: 6 temes + 3 treballs de recerca trimestrals.
- Caldrà assolir els continguts mínims per poder accedir amb garanties a un Cicle Superior.
PROGRAMACIÓ D’AULA
(adaptació del programa oficial proposat pel Departament d’Ensenyament:
—-
Presentació de l’assignatura.
UNITAT 1. CONCEPTES BÀSICS.
Fenòmens físics i químics. Diferència entre fenòmens físics i químics. Objectius de la química en quan a composició, estructura, energia, propietats i reactivitat. —-
La matèria. Estats de la matèria. Propietats (forma, volum i densitat). Classificació de la matèria: Substàncies pures i mescles. Substàncies pures: Elements (símbol) i compostos (fórmula). Nombre atòmic Z i massa atòmica A. Isòtops. Càlcul de la massa atòmica relativa.
—-
Quantitat de substància. Molècula. Massa molecular. Mol. Nombre d’Avogadro, NA. Intercanvi de magnituts (triàngle màgic). Elements (símbols): grams- a t-gr – àtoms. Compostos (molècules): gr – mols – molécules -àtoms. Tipus de fórmules químiques (empírica, molecular, semidesenvolupada i desenvolupada) Composició centesimal. Càlcul de la composició centesimal a partir de la fórmula i a l’inrevés.
—-
L’estat gasós. Estats d’agregació de la matèria: propietats (forma, volum, densitat). L’estat gasós. Lleis que regulen el comportament dels gasos (Boyle-Mariotte, Gay-Lussac, Charles). Equació general dels gasos. Equació dels gasos ideals.
—-
Condicions normals i condicions estàdard. Volum molar. Relació entre la densitat i la llei dels gasos. Mescles de gasos. Fracció molar. Pressió parcial d’un gas. Relació entre la pressió parcial i la pressió total.
****** Prova parcial P1 prevista pel 22 d’octubre *****
*****Hora: 17.30 hores – DURADA APROXIMADA : 60 minuts ******
Efectes del calor i la temperatura sobre la matèria. Escalfament (calor específica) i canvis d’estat (calor latent). Representació gràfica de l’efecte del calor amb i sense canvi d’estat.
Mescles (homogènies i heterogènies). Criteris de puresa. Mètodes de separació de mescles. Decantació, filtració, cristal•lització, destil•lació, extracció amb dissolvents i cromatografia. Aparells per a la separació de mescles: centrifugadora, embut de decantació i garbell o filtre.
—-
Les reaccions químiques. Estequiometria. Tipus de reaccions químiques. Lleis ponderals i volumètriques. Llei de Lavoisier. Igualació de reaccions químiques. Càlculs estequiomètrics. Reactiu sobrant i reactiu limitant
****** Prova parcial P2 prevista pel 26/11/14*****
*****Hora: 19.30 hores – DURADA APROXIMADA : 60 minuts ******
Models atòmics. Evolució de les teories atòmiques des de l’antiquitat fins els nostres dies. Teories atòmiques (Rutherford, Bohr i model quàntic actual) Concepte d’òrbita i d’ orbital. Breu menció als nombres quàntics (n, l, m i s) i el seu significat. Energia dels orbitals i configuració electrònica. Regla d’emplenat de Möeller. Classificació dels elements:
La taula periòdica (Grups i períodes). Propietats periòdiques (radi atòmic, volum atòmic, energia d’ionització, afinitat electrònica, electroafinitat , caràcter metàl·lic i electronegativitat
UNITAT 2. FORMULACIO I NOMENCLATURA I ENLLAÇ QUÍMIC.
Formulació i nomenclatura inorgànica. Valencia dels elements químics. L’ió amoni. Compostos binaris. Compostos ternaris. Sals àcides. Formulació i nomenclatura orgànica.
Principals funcions orgàniques. Compostos hidrogenats. Compostos oxigenats. Compostos nitrogenats.
(Caldrà saber distingir les diferents funcions orgàniques).
Enllaç químic i geometria molecular. Tipus d’enllaç químic (iònic, covalent – substàncies moleculars, H2 i substàncies atòmiques, C- , datiu o coordinat i metàl·lic). Estructura de Lewis (àtoms, ions i molècules). Formes ressonants. Teoria de la repulsió dels parells electrònics (geometria molecular). Enllaços polars i no polars (apolars). Enllaços intramoleculars i intermoleculars. Enllaços de Van der Waals i enllaç per ponts d’hidrogen.
****** Prova parcial P3 prevista pel 21/01/15 *****
*****Hora: 19.30 hores – DURADA APROXIMADA : 60 minuts ******
UNITAT 3. DISSOLUCIONS I SOLUBILITAT
Dissolucions. Concepte de dissolució. Conceptes de solut i dissolvent. Exemples dels diferents tipus de dissolucions. Preparació d’una dissolució. Concepte de solubilitat. Factors que influeixen en la solubilitat. Gràfiques solubilitat-temperatura. Tipus de dissolucions (Concentrada, diluïda, saturada i sobresaturada). Concepte de concentració. Mesura de la concentració (% massa, % volum, molaritat, molalitat, fracció molar, ppm). Propietats col·ligatives de les dissolucions (pressió de vapor, augment ebulloscòpic, descens crioscòpic, pressió osmòtica)
Solubilitat, Kps. Solubilitat dels compostos iònics. Solubilitat. Solució saturada. Factors que influeixen en la dissolució. Regles de solubilitat. Producte de solubilitat. Significat del Kps. Producte iònic. Relació entre la solubilitat i el Kps.Càlcul de Kps a partir de la solubilitat. Càlcul de la solubilitat a partir de Kps. Reaccions de precipitació. Predicció de la formació de precipitats.
Precipitació fraccionada. Efecte de l’ió comú sobre la solubilitat. Dissolució de precipitats. Variació de la temperatura. Addició de dissolvent. Formació d’electròlits dèbils. Formació d’un ió complex.
****** Prova parcial P4 prevista pel 04/03/15*****
*****Hora: 19.30 hores – DURADA APROXIMADA : 60 minuts ******
UNITAT 4. EQUILIBRIS QUÍMICS: EQUILIBRIS GASOSOS. EQUILIBRIS HETEROGENIS. SOLUBILITAT. EQUILIBRIS ÀCID-BASE.
Equilibris gasosos. Reaccions reversibles i irreversibles Característiques de l’estat d’equilibri.La constant d’equilibri Kc.Equilibris homogenis: llei d’acció de masses. Significat del valor de la constant KC.Relació entre Kc i l’equació ajustada.Deducció cinètica de la constant d’equilibri. Càlculs en equilibris homogenis en fase gasosa. El quocient de reacció.Equilibris heterogenis.Energia lliure i constant d’equilibri.Alteració de l’equilibri. Principi de Le Chatelier.Canvis en la concentració.Canvis de pressió per variació de volum.Canvis de temperatura.
Aplicació a la síntesi industrial de l’amoníac. Factors que influeixen en la velocitat de reacció.Temperatura de la reacció.Concentració dels reactius. Naturalesa, estat físic i grau de divisió.
Reaccions acid-base i pH.Introducció històrica sobre l’evolució dels conceptes d’àcid i base.Teoria d’Arrhenius.La dissociació iònica.Àcids i bases.Neutralització.Teoria de Brönsted-Lowry.Àcid i base conjugats. Amfoterisme.Comparació amb la teoria d’Arrhenius. Autoionització de l’aigua.Força dels àcids i de les bases.Àcids i bases forts i dèbils.Relació entre l’àcid i la seva base conjugada.Constant d’ionització d’àcids i bases dèbils.Predicció de les reaccions àcid-base.Relació entre la força d’àcids i bases i l’estructura molecular.Àcids i bases dèbils: constants d’ionització.Ionització d’un àcid dèbil.Ionització d’una base dèbil.Relació entre les constants Ka, Kb i Kw.El grau d’ionització en el càlcul de Ka i Kb.. Àcids polipròtics.Relació entre les diferents constants de l’àcid.El pH de les solucions aquoses.Conceptes de pH i pOH.Soluciones neutres, àcides i bàsiques.Escala de pH.El pH d’àcids forts i de bases fortes. Solucions amortidores o reguladores. Efecte de l’ió comú.
Actuació de les solucions reguladores. El pH de les solucions reguladores. Indicadors àcid-base.Mecanisme de funcionament.Hidròlisi de les sals.Sals de base forta i àcid fort.Sals de base forta i àcid dèbil.Sals de base dèbil i àcid fort.Sals de base dèbil i àcid dèbil.Grau d’hidròlisi.Valoracions àcid-base.Corbes de valoració.
****** Prova parcial P5 prevista pel 15/04/15*****
*****Hora: 19.30 hores – DURADA APROXIMADA : 60 minuts ******
UNITAT 5. BIOQUÍMICA BÀSICA (I): BIOELEMENTS. HIDRATS DE CARBONI, LÍPIDS, PROTEÏNES I ÀCIDS NUCLEICS
Els Bioelements. Les Biomolécules. L’aigua. Les sals minerals. Els glúcids. Monosacàrids. Oligosacàrids. Polisacàrids. Funcions dels glúcids. Els lípids. Ácids grasos. Acilglicérids. Ceres . Fosfoglicérids i esfingolípids. Esteroides. Isoprenoides . Prostaglandines. Les proteïnes. Aminoàcids. Péptids . Estructura de les proteïnes. Funcions de las proteïnes. Els Àcids Nuclèics. Nucleòtids. ADN. ARN.
UNITAT 6. BIOQUÍMICA BÀSICA (II): METABOLISME.
Consideracions generals sobre metabolisme.El catabolisme.El catabolisme aerobic. Glucòlisis.Respiració celul·lar: cicle de Krebs.Cadena respiratòria: hipótesi quimiosmòtica.Fermentacions. Oxidació dels ácidos grasos: ß-oxidació dels àcids grasos.Oxidació dels aminoàcids.L’anabolisme. Pigments, fotosistemes y fotosíntesi.Fase lluminosa de la fotosíntesi.Fase fosca de la fotosíntesi. Factors que influeixen en la fotosíntesi.Quimiosíntesi.
****** Prova parcial P6 prevista pel 20/05/15 *****
*****Hora: 19.30 hores – DURADA APROXIMADA : 60 minuts ******
Treballs monogràfics i de recerca (seran imprescindibles per a aprovar l’assignatura – valoració màxima: 1 punt sobre la nota del trimestre). Se’n farà un per trimestre. Es lliuraran la mateixa setmana del segon examen trimestral.
- Document word (màx 25 pàgines) – format .doc (format obligatòri)
- (si voleu podeu lliurar també una versió addicional en pdf, independentment de que es presenti el document en word)
- PowerPoint (entre 20 i 25 diapositives) – format .ppt
- Cal que hi figuri la bibliografia i/o pàgines web consultades (tant pel texte com per a les imatges emprades)
- Vigileu que el format sigui el correcte*
FORMAT dels fitxers adjunts: Pels documents SEMPRE .doc i pels PowerPoint el format serà SEMPRE .ppt (no s’admet cap altre format!)
APARTAT ASSUMPTE: CAS-XXX-TITOL (XXX són les vostres inicials)
NOM DELS DOCUMENTS: Documents en Word: CAS-XXX-TITOL.doc Presentacions en PowerPoint: CAS-XXX-TITOL.ppt COS DEL MISSATGE: Nom Cognom1 Cognom2
*La no presentació del format correcte pot suposar considerar el treball com a NO LLIURAT i la no presentació dels treballs obligatoris pot suposar suspendre l’assignatura.
Els treballs es valoraran fins a el 10% de la nota del trimestre (com en el cas dels treballs de recerca de Batxillerat). Es a dir poden pujar un màxim d’un punt la nota del trimestre.
ELS TITOLS I CONTINGUT DELS TREBALLS A LLIURAR AL FINAL DE CADA TRIMESTRE SÓN:
A. De la cèl·lula a un organisme. La cél·lula: unitat d’estructura i funció.
(Setmana del 26/11/14)
Diferencia la cèl·lula eucariota i procariota i reconeix l’estructura i funcions dels orgànuls cel·lulars. Identifica l’estructura i la funció d’algunes cèl·lules especialitzades: secretores, musculars, nervioses. Identifica en esquemes o representacions les fases del cicle cel•lular, i explica les diferencies i el significat de la mitosi i meiosi. Descriu els mecanismes que controlen el cicle cel·lular i la disfunció en les cèl·lules canceroses.
B. Els bacteris i virus en acció.
Identifica la morfologia i estructura dels virus i relaciona replicació del material hereditari amb les infeccions víriques. Identifica les implicacions en la salut individual i col·lectiva d’algunes malalties víriques i reconeix les mesures de prevenció. Identifica la morfologia i estructura bacteriana, relaciona el procés d’autoduplicació, i reconeix algunes de les aplicacions dels bacteris. Reconeix la presència dels bacteris en la vida quotidiana i algunes de les seves aplicacions en processos industrials: agricultura, farmàcia i alimentació. Relaciona la utilització dels antibiòtics amb els seus efectes sobre la salut i els problemes de resistència que es generen amb l’ús inadequat. Explica de forma esquemàtica les reaccions antigen i anticòs com a mecanismes de defensa que desenvolupa l’organisme. Relaciona els processos del sistema immune amb les vacunes, els processos al·lèrgics i el càncer.
(Setmana del 04/03/15)
C. La biodiversitat.
Classifica els organismes en els cinc regnes a partir de les seves característiques morfoanatòmiques i fisiològiques. Identifica alguns mecanismes de l’evolució i l’aparició o desaparició d’espècies com la selecció natural o processos genètics. Reconeix la importància del manteniment de la biodiversitat i indica accions per a la conservació d’espècies en perill d’extinció.
(Setmana del 20/05/15)
BIBLIOGRAFIA:
Apunts de classe (Font principal)
- Llibres de primer i segon de batxillerat de química
- Llibres de primer i segon de batxillerat de biologia.
Altres fonts:
- Projecte BIOSFERA (MEC): recursostic.educacion.es/ciencias/biosfera/web
- http://recursostic.educacion.es/ciencias/biosfera/web/profesor/1bachillerato/1.htm
- http://recursostic.educacion.es/ciencias/biosfera/web/profesor/2bachillerato/1.htm
- http://roble.pntic.mec.es/epam0023/videospaginasseleccionadas.pdf
FORMAT pels fitxers adjunts: SEMPRE .doc (no s’admet cap altre format!)
pels PowerPoint el format serà SEMPRE .ppt
APARTAT ASSUMPTE: CAS-XXX-TITOL (XXX són les vostres inicials)
NOM DELS DOCUMENTS:
Documents en Word: CAS-XXX-TITOL.doc
Presentacions en PowerPoint: CAS-XXX-TITOL.ppt
COS DEL MISSATGE: Nom Cognom1 Cognom2
La no presentació del format correcte pot suposar considerar el treball com a NO LLIURAT.
La no presentació dels treballs obligatoris pot suposar suspendre l’assignatura.
Els treballs es valoraran amb el 10% de la nota (com en el cas dels treballs de recerca de Batxillerat). Es a dir poden pujar un màxim d’un punt la nota del trimestre.
CLIQUEU A FORMAT PERVEURE COM GUARDAR COM A UN DOCUMENT .doc
Pels powerpoint feu servir el format compatible ppt
Des de Microsoft Office hi ha la opció directa: Guardar com .ppt
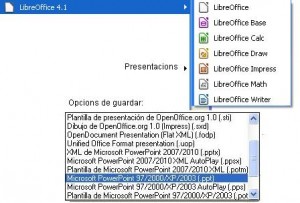
Des de Llibre Office el podeu posar aixi:
PRIMER MISSATGE DE PRESENTACIÓ
APARTAT ASSUMPTE: CAS-XXX_PRESENTACIÓ (XXX són les vostres inicials)
COS DEL MISSATGE: Nom Cognom1 Cognom2
TREBALLS TRIMESTRALS:
El format a l’apartat assumpte serà: CAS-XXX-TITOL, tot en majúscules. El titol s’indicarà en el bloc i XXX representen les vostres inicials.
L’hora de lliurament dels treballs és fins les 23.59 del dia fixat. No s’admetran treballs fora de termini.
TITOLS DELS TREBALLS COMPLEMENTARIS:
1r Trimestre: La cèl·lula.
2n Trimestre: Bacteris i virus.
3r Trimestre: Biodiversitat.